Лаборатория биотехнологий
Лаборатория биотехнологий в составе Университетской клиники ФГБОУ ВО «ПИМУ» Минздрава России была выделена в самостоятельное подразделение в 2016 году.
На сегодняшний день лаборатория успешно прошла аудит по стандартам ISO 9001-2015 и готова к сертификации по GLP-стандарту, так же запланирована аккредитация на соответствие требованиям ISO/IEC 17025-2019.
Деятельность лаборатории охватывает широкий спектр исследований, посвященных изучению и применению соматических клеток человека и животных и разработке материалов биомедицинского назначения.
Эти исследования лежат в основе разработки высокотехнологичных лекарственных препаратов на основе соматических клеток и технологий лечения, базирующихся на использовании свежевыделенных клеток человека, проведения комплексных доклинических исследований материалов для медицинского применения, работах в области скаффолд-технологий.
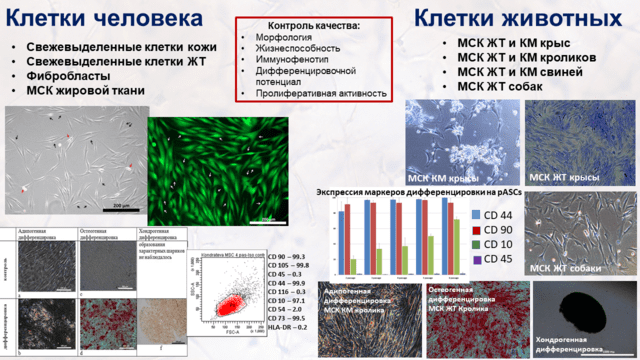
Для разработки и доклинических исследований клеточных продуктов и различных материалов и в качестве тест-систем в лаборатории используются первичные культуры фибробластов и стволовых клеток человека, культуры стволовых клеток животных (крысы, кролика, свиньи и др.). Стволовые клетки животных также используются при проведении исследований in vivo в соответствии со стратегией "гомологичный препарат".
Важнейшая задача лаборатории
- История лаборатории
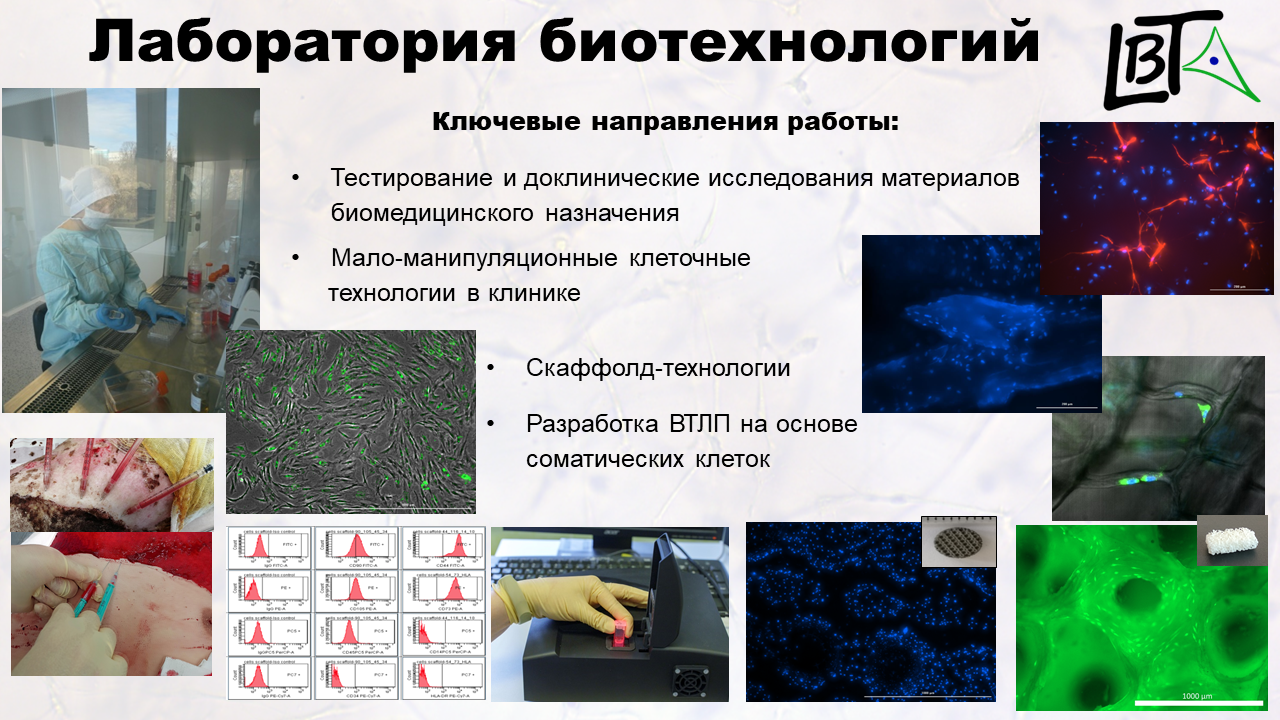
- Направления работы
- Оснащение лаборатории
- Гранты, государственные задания, договорные работы, реализуемые проекты
- Патенты
- Ключевые публикации сотрудников лаборатории
- Контакты и предложения сотрудничества
Лаборатория биотехнологий продолжает работу, которую ранее в составе отделения консервации тканей выполняла группа биотехнологий. В 1988 году в структуре лаборатории консервации тканей Нижегородского института травматологии и ортопедии была создана группа под руководством к.м.н. Дианы Яковлевны Алейник, задачей которой было наладить работу с культурами клеток кожи для лечения ожогов и ран. Уже в январе 1991 года клеточные трансплантаты были успешно использованы для лечения ожоговых ран у первого пациента и с этого времени активно применялись в комплексном лечении пациентов Ожогового центра института.
Сотрудниками лаборатории и ожогового центра накоплен опыт использования клеточной терапии более чем у 2000 тысяч пациентов с ожоговыми и длительно незаживающим ранами различного генеза. На основе совместной работы сотрудниками института защищено 3 кандидатские и одна докторская диссертации.
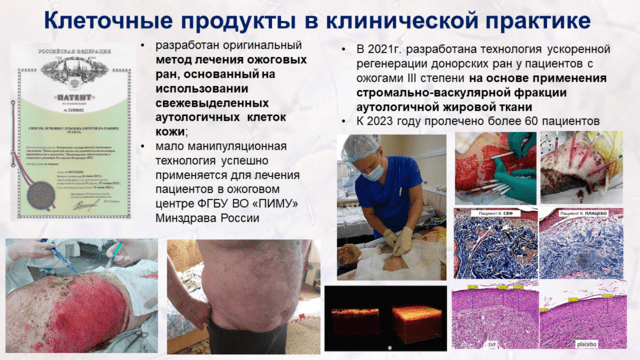
В лаборатории в сотрудничестве со специалистами ожогового центра Университетской клиники разработан оригинальный метод лечения ожоговых ран, основанный на использовании свежевыделенных аутологичных клеток кожи (Карякин Н.Н., Докукина Л.Н., Алейник Д.Я. и др. Способ лечения глубоких ожогов на ранних этапах. Патент РФ №2499603; 2013). Эта маломанипуляционная технология успешно применялась для лечения ожоговых поражений кожи у пациентов разного возраста в ожоговом центре ФГБОУ ВО «ПИМУ» Минздрава России, а также в других клиниках (например, в Детском ожоговом центре больницы № 9, г. Москва).
В 2016 г. лаборатория биотехнологий была перебазирована в новое здание Института педиатрии Университетской клиники ФГБОУ ВО «ПИМУ» Минздрава России, где организована чистая зона площадью более 100 м2. и криобанк для хранения культур клеток. В 2019 г. руководство лабораторией было передано к.б.н. Егорихиной Марфе Николаевне. В 2021 г. в лаборатории биотехнологий был выделен бокс с изолированной вентиляционной системой для работы с клетками животных. За этот период лаборатория была укомплектована комплексом исследовательского оборудования, в том числе рядом уникальных приборов (см. раздел Оснащение лаборатории).
Продолжением работы с ожоговыми поражениями кожи стала реализация на базе лаборатории темы Государственного задания: «Разработка методов восстановления раневых дефектов кожного покрова путем создания биомедицинского клеточного продукта и оптимизации условий репарации» (2018 – 2020 гг.). В рамках выполнения указанной темы Государственного задания в лаборатории был разработан оригинальный биомедицинский клеточный продукт (Егорихина М.Н. с коллегами – Патент РФ №2653434 RU) – эквивалент для восстановления дефектов кожи, и проведены комплексные доклинические исследования на животных моделях (крысы, свиньи), подтвердившие безопасность и эффективность разработанного эквивалента кожи.
Лаборатория принимает активное участие в клинической работе. Совместно с специалистами ожогового центра ПИМУ, в рамках программы «Приоритет-2030», была разработана технология лечения донорских ран пациентов с ожоговой травмой на основе использования аутологичной свежевыделенной фракции клеток жировой ткани (СВФ). СВФ была использована у 60 пациентов первого ожогового отделения взрослых Университетской клиники.
Аутологичные свежевыделенные клетки жировой ткани и кожи, полученные в лаборатории биотехнологий, применяются у пациентов с ожоговой травмой в сочетании с высоко перфорированными аутотрансплантатами для стимуляции регенерации и ускорения эпителизации в области ожогового повреждения кожного покрова.
На базе лаборатории совместно с ИМХ РАН, ННГУ им. Н.И. Лобачевского, ФГБОУ ВО «УУНиТ», ООО "АйконЛаб Гмбх" и др. проводятся исследования различных материалов биомедицинского назначения (коснозамещающие материалы, раневые покрытия, имплантаты для стоматологии, травматологии и ортопедии и т.д.) и покрытий для имплантатов. На базе лаборатории разработан и реализуется обширный комплекс методов для проведения доклинических исследований in vitro медицинских изделий, материалов биомедицинского назначения, лекарственных препаратов и ВТЛП на основе соматических клеток и их продуктов.
В настоящее время лаборатория активно расширяет сферу своей деятельности. В 2022 г. лаборатория успешно прошла сертификацию на соответствие стандарту ISO 9001-2015. Деятельность лаборатории осуществляется в соответствии со стандартами GLP. Планируется аккредитация лаборатории по ГОСТ ISO/IEC 17025-2019.
• Тестирование материалов биомедицинского назначения

• Разработка маломанипуляционных клеточных технологий для медицины
• Разработка продуктов для восстановления раневых дефектов кожи

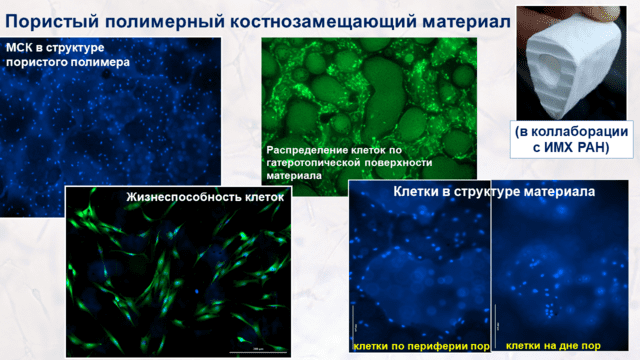
• Разработка костнозамещающих материалов
• Оценка цитотоксического действия лекарственных препаратов in vitro МТТ-тест, метод прямого контакта
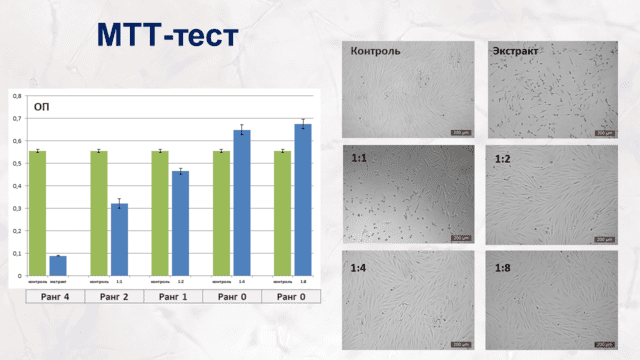
• Исследования in vivo на мелких и крупных лабораторных животных


2. Выделен отдельный бокс для работы с клетками животных, оборудованный в соответствии со стандартами GМP. Бокс оснащен индивидуальной вентиляционной системой, что исключает пересечение генетического материала человека и животных при работе.

3. Комната имиджинга с уникальным оборудованием для прижизненной визуализации клеток и их структур: многофункциональный имиджер Cytation 5 с программным обеспечением Gen 5 Imedge+ (BioTek, USA), имиджер Image Ex Fluorer с модулем искусственного интеллекта (Live Cell Instrument Inc., Республика Корея). Имиджеры позволяют оценить адгезию клеток на материалы, жизнеспособность и пролиферативную активность клеток при взаимодействии с материалами, миграцию клеток в структуру трехмерных материалов.
имиджер Image Ex Fluorer с модулем искусственного интеллекта (Live Cell Instrument Inc., Республика Корея) многофункциональный имиджер Cytation 5 с программным обеспечением Gen 5 Imedge+ (BioTek, USA)

4. Цитофлуориметр Becton Dikinson для реализации метода проточной цитометрии для клинического применения (исследования иммунного статуса) и для исследовательских целей (подтверждение качества культур поверхностно-зависимых клеток, оценка изменений иммунофенотипа клеток при взаимодействии с материалами или лекарственными препаратами).

5. Ультрацентрифуга и счетчик наночастиц – используются для выделения и подсчета микро- и наноструктур клеток и наночастиц с характеристикой частиц при по фракциям и количеству.

Настольная ультрамикроцентрифуга himac CS150NX (Hitachi Koki, Япония). Анализатор размеров и счётной концентрации наночастиц АРНмини

6. Оборудование для проведения иммуноферментного анализа (фотометр InfiniteF50 c программным обеспечением Magellan Tracker (Tecan Austria GmbH, Австрия), прибор для промывки микропланшет HydroFlex TECAN (Tecan, Австрия) – позволяет реализовывать методы, в основе которых лежит изменение оптической плотности исследуемых растворов. Одним из базовых методов является оценка цитотоксичности методом МТТ-теста, рекомендованным ГОСТ ISO 10993-5-2011. Иммуноферментный анализ широко используется для оценки секреторной активности клеток при взаимодействии с медицинскими изделиями, материалами и лекарственными препаратами.

7. Криобанк, оснащенный криохранилищем, аппаратурой для программного замораживания, морозильным оборудованием на –40°С, –80°С, –150°С и дьюарами с жидким азотом (–196°С).

- Грант РНФ №20-79-10189-П «Моделирование и диагностика процесса плазменно-электролитического оксидирования для разработки smart-технологии формирования покрытий медицинских имплантатов из наноструктурированного циркония» (2023-2025 гг; грантодержатель ФГБОУ ВО «УУНиТ»)
- Приоритет-2030 стратегический проект «Трансляционная регенеративная медицина» (2021-2030гг.).
- Государственное задание «Новые биосовместимые и биорезорбируемые полиэфиры для мседицины» (Грантодержатель НГПУ им. К. Минина)
- Грант РНФ № 22-23-20091 «Разработка химической модели гибридного материала для регенеративной медицины (скаффолда) на основе морского коллагена и синтетических полимеров» (2022-2023 гг.; грантодержатель ННГУ им. Лобачевского)
- Государственное задание «Разработка технологий, повышающих эффективность декомпрессивно-стабилизирующих вмешательств, с применением транспедикуляторной фиксации и костной пластики у пациентов с дегенеративной патологией и травматическими повреждениями позвоночника» (2021-2024гг.)
- Государственное задание: «Разработка технологий восстановления раневых дефектов кожного покрова с применением оригинального биомедицинского клеточного продукта и мало манипуляционных клеточных технологий» (2021 – 2023гг.).
- Договор на выполнение НИР с AHO «Нижегородский НОЦ» по теме «Разработка комплексного подхода к оценке биосовместимости in vitro материалов биомедицинского назначения» (2020г).
- Государственное задание: «Разработка методов восстановления раневых дефектов кожного покрова путем создания биомедицинского клеточного продукта и оптимизации условий репарации» (2018 – 2020гг).
- Грант РНФ № 18-13-00434 «Гибридные органические материалы для синтеза персонифицированных костнозамещающих имплантатов с использованием аддитивных технологий» (2018 - 2020 гг; грантодержатель ИМХ РАН).
- Государственное задание «Разработка персонифицированного подхода к лечению гнойно-воспалительных заболеваний костной ткани на основании факторов естественного и адаптивного иммунитета и методов тканезаместительной терапии» (2017-2019гг.).
- Федеральная целевая программа «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014-2020 годы», в рамках выполнения НИР «Разработка технологии производства, хранения и применения биомедицинских клеточных продуктов для лечения ран» (уникальный идентификатор работ RFMEFI61017X0012; грантодержатель ИБР РАН).
- Государственный контракт № 16.522.11.2010 от 20.06.12 «Разработка технологии получения композиционного костнозамещающего материала для стоматологии, челюстно-лицевой хирургии и травматологии» (Шифр «2012 – 2.2.- 16.- 522 – 0016).
- Грант Нижегородской области: «Создание нового биоактивного материала на основе наноразмерного гидроксиапатита для медицинских целей»;
- Заявка на патент №2023132910 от 12.12.2023: СПОСОБ ОЦЕНКИ ДИФФЕРЕНЦИРОВКИ МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК В ТРЁХМЕРНЫХ СКАФФОЛДАХ \\ М.Н. Егорихина, Д.Д. Линькова, И.Н. Чарыкова
- Пат. RU2792566C1 Устройство для забора подкожной жировой ткани у пациентов с обширными ожогами кожи // Рябков Максим Георгиевич, Колошеин Никита Анатольевич, Лузан Александр Сергеевич, Егорихина Марфа Николаевна, Бесчастнов Владимир Викторович, Марков Сергей Николаевич – № 2022132665/14(071206), Заяв. 13.12.2022. Опубл.22.03.2023г
- Пат. 2777257 РФ, СПК G01N 33/52 (2022.05); A61B 5/00 (2022.05) Способ определения жизнеспособности клеток в биомедицинских клеточных продуктах в процессе регенерации // Егорихина М.Н. (РФ), Чарыкова И.Н. (РФ), Алейник Д.Я. (РФ), Рубцова Ю.П. (РФ) – №2021108641, Заяв. 30.03.2021; Опубл. 01.08.2022; Бюл. № 22
- Пат. RU 2795239 C1 RU (11) 2 795 239(13) C1 РОССИЙСКАЯ ФЕДЕРАЦИЯ (51) МПК C12N 5/0775 (2010.01) Способ скрининговой оценки пролиферативной активности клеток в процессе роста // Обухова Л. М., Никифорова О. Н., Егорихина М. Н., Алейник Д. Я., Чарыкова И.Н. - Заявка № 2022108913 от 04.04.2022; Опубл. 02.05.2023 Бюл. № 13
- Пат. 2758863 РФ, МПК C08F 2/46 (2006.01), A61F 2/02 (2006.01), A61L 27/14 (2006.01); СПК C08F 2/46 (2021.05), A61F 2/02 (2021.05), A61L 27/14 (2021.05) Способ получения полимерного материала для замещения дефектов кости // Ковылин Р.С. (RU), Егорихина М.Н. (RU), Юдин В.В. (RU), Чесноков С.А. (RU), Алейник Д.Я. (RU), Рубцова Ю.П. (RU), Заславская М.И. (RU), Млявых С.Г. (RU), Федюшкин И.Л. (RU) – Заявка №2020124050, 13.07.2020; Опубл. 02.11.2021; Бюл. № 31
- Пат. 2740566 РФ, МПК G01N 21/64, G01N 1/30 Способ оценки миграции клеток в структуру материала или скаффолда // Егорихина М.Н. (РФ), Рубцова Ю.П. (РФ), Алейник Д.Я., Чарыкова И.Н., Ковылин Р.С., Юдин В.В., Чесноков С.А.- №2020119705; Заяв. 08.06.2020; Опубл. 15.01.2021; Бюл. №2
- Пат. 2695061 РФ, МПК А61L 27/14 Способ характеристики пористости скаффолдов и/или клеточно-инженерных конструкций // Егорихина М.Н. (РФ), Рубцова Ю.П. (РФ), Бугрова М.Л. (РФ) – №201912633; Заяв. 25.04.2019; Опубл. 19.07.2019; Бюл. №20
- Пат. 2683322 РФ, МПК G01N 33/48, А61К 35/18, А61К 9/52 Способ пролонгированного высвобождения биологически активных веществ из теней эритроцитов // Левин Г.Я. (РФ), Егорихина М.Н. (РФ), Соснина Л.Н. (РФ), Чарыкова И.Н. (РФ), Рубцова Ю.П. (РФ) – №2018103117; Заяв. 26.01.2018; Опубл. 28.03.2019; Бюл. №10
- Пат. 2675376 РФ, МПК G01N 33/52 Способ количественного анализа клеточной составляющей скаффолда // Егорихина М.Н. (РФ), Чарыкова И.Н. (РФ), Алейник Д.Я. (РФ) – №2017125696; Заявл. 17.07.2017; Опубл. 19.12.2018; Бюл. №35.
- Пат. 2665155 РФ, МПК А61К 47/00, А61К 9/52. Способ доставки биологически активных веществ в скаффолд // Левин Г.Я. (РФ), Егорихина М.Н. (РФ), Соснина Л.Н. (РФ), Чарыкова И.Н. (РФ), Алейник Д.Я. (РФ) – №2018100730; Заяв. 10.01.2018; Опубл. 28.08.2018; Бюл. №25
- Пат. 2653434 РФ, МПК C12N 5/00. Способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови / Егорихина М.Н. (РФ), Левин Г.Я. (РФ), Чарыкова И.Н. (РФ), Алейник Д.Я. (РФ), Соснина Л.Н. (РФ). — № 2017112424; Заяв. 11.04.2017; Опубл. 08.05.2018; Бюл. № 13. — 13 с., ил.
- Пат. 2653476 РФ, МПК G01N 33/48. Способ микроскопической оценки цитотоксичности компонентов материалов скаффолдов / Левин Г.Я. (РФ), Егорихина М.Н. (РФ), Соснина Л.Н. (РФ), Шереметьев Ю.А. (РФ), Чарыкова И.Н. (РФ) — № 2017116313; Заяв. 10.05.2017; Опубл. 08.05.2018; Бюл. № 13. — 10 с., ил
- Пат. RU 2624230 C Способ лечения больных при острой стадии диабетической нейростеоартропатии по типу "стопа шарко" // Бобров М.И., Митрофанов В.Н., Шаталин А.Е., Алейник Д.Я. – Заявка № 2016128696 от 13.07.2016; Опубл. 03.07.2017.
- Пат. RU 2499603 C1 Способ лечения глубоких ожогов на ранних этапах // Карякин Н.Н., Докукина Л.Н., Алейник Д.Я., Аминев В.А., Квицинская Н.А., Соколов Р.А. – Заявка № 2012122660/15 от 01.06.2012; Опубл. 27.11.2013.
-
Egorikhina, M.N.; Rubtsova, Y.P.; Linkova, D.D.; Charykova, I.N.; Farafontova, E.A.; Aleinik, D.Y. Specifics of Cryopreservation of Hydrogel Biopolymer Scaffolds with Encapsulated Mesenchymal Stem Cells. Polymers 2024, 16, 247. https://doi.org/10.3390/polym16020247
-
Semenycheva, L.; Chasova, V.O.; Pegeev, N.L.; Uromicheva, M.A.; Mitin, A.V.; Kuznetsova, Y.L.; Farafontova, E.A.; Rubtsova, Y.P.; Linkova, D.D.; Egorikhina, M.N. Production of Graft Copolymers of Cod Collagen with Butyl Acrylate and Vinyl Butyl Ether in the Presence of Triethylborane—Prospects for Use in Regenerative Medicine. Polymers 2023, 15, 3159. https://doi.org/10.3390/polym15153159
-
Beschastnov, V.V.; Egorikhina, M.N.; Tulupov, A.A.; Pogodin, I.E.; Orlinskaya, N.Y.; Antoshina, V.V.; Shirokova, I.Y.; Ryabkov, M.G. Immobilization of Bacteriophages in Ex Tempore Hydrogel for the Treatment of Burn Wound Infection. Gels 2023, 9, 625. https://doi.org/10.3390/gels9080625
-
Kuznetsova, Y.L.; Gushchina, K.S.; Lobanova, K.S.; Chasova, V.O.; Egorikhina, M.N.; Grigoreva, A.O.; Malysheva, Y.B.; Kuzmina, D.A.; Farafontova, E.A.; Linkova, D.D.; et al. Scaffold Chemical Model Based on Collagen—Methyl Methacrylate Graft Copolymers. Polymers 2023, 15, 2618. https://doi.org/10.3390/polym15122618
-
Egorikhina, M.N.; Timofeeva, L.B.; Linkova, D.D.; Rubtsova, Y.P.; Bugrova, M.L.; Charykova, I.N.; Ryabkov, M.G.; Kobyakova, I.I.; Farafontova, E.A.; Aleynik, D.Y. Biocompatibility Study of Hydrogel Biopolymer Scaffold with Encapsulated Mesenchymal Stem Cells. Polymers 2023, 15, 1337. https://doi.org/10.3390/polym15061337
-
Egorikhina MN, Kobyakova II, Charykova IN, Linkova DD, Rubtsova YP, Farafontova EA, Aleynik DY. Application of hydrogel wound dressings in cell therapy-approaches to assessment in vitro. Int J Burns Trauma. 2023 Apr 15;13(2):13-32. PMID: 37215513; PMCID: PMC10195216.
-
Egorikhina, M.N.; Bokov, A.E.; Charykova, I.N.; Rubtsova, Y.P.; Linkova, D.D.; Kobyakova, I.I.; Farafontova, E.A.; Kalinina, S.Y.; Kolmogorov, Y.N.; Aleynik, D.Y. Biological Characteristics of Polyurethane-Based Bone-Replacement Materials. Polymers 2023, 15, 831. https://doi.org/10.3390/polym15040831
-
Yudin, V.V.; Shurygina, M.P.; Egorikhina, M.N.; Aleynik, D.Y.; Linkova, D.D.; Charykova, I.N.; Kovylin, R.S.; Chesnokov, S.A. Pore Structure Tuning of Poly-EGDMA Biomedical Material by Varying the O-Quinone Photoinitiator. Polymers 2023, 15, 2558. https://doi.org/10.3390/polym15112558
-
Kuznetsova, Y.L.; Sustaeva, K.S.; Mitin, A.V.; Zakharychev, E.A.; Egorikhina, M.N.; Chasova, V.O.; Farafontova, E.A.; Kobyakova, I.I.; Semenycheva, L.L. Graft Polymerization of Acrylamide in an Aqueous Dispersion of Collagen in the Presence of Tributylborane. Polymers 2022, 14, 4900. https://doi.org/10.3390/polym14224900
-
Semenycheva LL, Egorikhina MN*, Chasova VO, Valetova NB, Fukina DG, Sukhareva AA, Ostrosablin AN, Kobyakova II, Farafontova EA and Yu P Rubtsova. An Environmentally Friendly Solution Related to the Use of Fish Production Waste to Manufacture New Materials for Biomedicine. Examines Mar Biol Oceanogr. 5(1). EIMBO. 000606. 2022. DOI: 10.31031/EIMBO.2022.05.000606
-
Linkova, D.D.; Rubtsova, Y.P.; Egorikhina, M.N. Cryostorage of Mesenchymal Stem Cells and Biomedical Cell-Based Products. Cells 2022, 11, 2691. https://doi.org/10.3390/cells11172691
-
Kuznetsova, Y.; Gushchina, K.; Sustaeva, K.; Mitin, A.; Egorikhina, M.; Chasova, V.; Semenycheva, L. Grafting of Methyl Methacrylate onto Gelatin Initiated by Tri-Butylborane—2,5-Di-Tert-Butyl-p-Benzoquinone System. Polymers 2022, 14, 3290. https://doi.org/10.3390/polym14163290
-
Elnara R. Zhiganshina, Maxim V. Arsenyev, Dmytro A. Chubich, Danila A. Kolymagin, Anastasia V. Pisarenko, Dmitry S. Burkatovsky, Evgeny V. Baranov, Alexei G. Vitukhnovsky, Andrew N. Lobanov, Rilond P. Matital, Diana Ya. Aleynik, Sergey A. Chesnokov, Tetramethacrylic benzylidene cyclopentanone dye for one- and two-photon photopolymerization, European Polymer Journal, Volume 162, 2022, 110917, ISSN 0014-3057, https://doi.org/10.1016/j.eurpolymj.2021.110917.
-
Bulanov EN, Stasenko KS, Golitsyna ON, Egorikhina MN, Aleynik DY, Skoblikow NE, Knyazev AV. Crystal-chemical and morphological interpretation of the biocompatibility of compounds in a Ca-Na-Bi-fluorapatite system. Dalton Trans. 2022 Jan 17;51(3):969-977. doi: 10.1039/d1dt03558d. PMID: 34931203.
-
Egorikhina, M.N.; Bronnikova, I.I.; Rubtsova, Y.P.; Charykova, I.N.; Bugrova, M.L.; Linkova, D.D.; Aleynik, D.Y. Aspects of In Vitro Biodegradation of Hybrid Fibrin–Collagen Scaffolds. Polymers 2021, 13, 3470. https://doi.org/10.3390/polym13203470
-
Chasova, V., Semenycheva, L., Egorikhina, M. et al. Cod Gelatin as an Alternative to Cod Collagen in Hybrid Materials for Regenerative Medicine. Macromol. Res. 30, 212–221 (2022). https://doi.org/10.1007/s13233-022-0017-9
-
Egorikhina, M.N.; Semenycheva, L.L.; Chasova, V.O.; Bronnikova, I.I.; Rubtsova, Y.P.; Zakharychev, E.A.; Aleynik, D.Y. Changes in the Molecular Characteristics of Bovine and Marine Collagen in the Presence of Proteolytic Enzymes as a Stage Used in Scaffold Formation. Mar. Drugs 2021, 19, 502. https://doi.org/10.3390/md19090502
-
·Egorikhina, M.N.; Rubtsova, Y.P.; Aleynik, D.Y. Long-Term Cryostorage of Mesenchymal Stem Cell-Containing Hybrid Hydrogel Scaffolds Based on Fibrin and Collagen. Gels 2020, 6, 44. https://doi.org/10.3390/gels6040044
-
Bulanov, E.N., Stasenko, K.S., Aleynik, D.Y. et al. Making bioceramics from CaBiPO-apatite. Bull Mater Sci 44, 17 (2021). https://doi.org/10.1007/s12034-020-02324-y
-
Chesnokov SA, Aleynik DY, Kovylin RS, Yudin VV, Egiazaryan TA, Egorikhina MN, Zaslavskaya MI, Rubtsova YP, Gusev SA, Mlyavykh SG, Fedushkin IL. Porous Polymer Scaffolds based on Cross-Linked Poly-EGDMA and PLA: Manufacture, Antibiotics Encapsulation, and In Vitro Study. Macromol Biosci. 2021 May;21(5):e2000402. doi: 10.1002/mabi.202000402. Epub 2021 Mar 23. PMID: 33759338.
-
Marfa N. Egorikhina, Diana Ya Aleynik, Yulia P. Rubtsova, Irina N. Charykova, Quantitative analysis of cells encapsulated in a scaffold, MethodsX, Volume 7, 2020, 101146, ISSN 2215-0161, https://doi.org/10.1016/j.mex.2020.101146.
-
Morozov, A.G., Razborov, D.A., Egiazaryan, T.A. et al. In Vitro Study of Degradation Behavior, Cytotoxicity, and Cell Adhesion of the Atactic Polylactic Acid for Biomedical Purposes. J Polym Environ 28, 2652–2660 (2020). https://doi.org/10.1007/s10924-020-01803-x
-
Egorikhina, M.N.; Rubtsova, Y.P.; Charykova, I.N.; Bugrova, M.L.; Bronnikova, I.I.; Mukhina, P.A.; Sosnina, L.N.; Aleynik, D.Y. Biopolymer Hydrogel Scaffold as an Artificial Cell Niche for Mesenchymal Stem Cells. Polymers 2020, 12, 2550. https://doi.org/10.3390/polym12112550
-
Semenycheva LL, Egorikhina MN, Chasova VO, Valetova NB, Kuznetsova YL, Mitin AV. Enzymatic Hydrolysis of Marine Collagen and Fibrinogen Proteins in the Presence of Thrombin. Mar Drugs. 2020 Apr 11;18(4):208. doi: 10.3390/md18040208. PMID: 32290502; PMCID: PMC7230862.
-
Bulanov, E., Silina, N., Lelet, M. et al. Study of physicochemical properties of nanohydroxyapatite–chitosan composites. Bull Mater Sci 43, 91 (2020). https://doi.org/10.1007/s12034-020-2065-0
-
Yudin V. V. et al. Visible-light induced synthesis of biocompatible porous polymers from oligocarbonatedimethacrylate (OСM-2) in the presence of dialkyl phthalates // Polymer. 2020. Vol. 192. p. 122302.
-
Marfa N. Egorikhina, Diana Ya Aleynik, Yulia P. Rubtsova, Grigory Ya Levin, Irina N. Charykova, Ludmila L. Semenycheva, Marina L. Bugrova, Evgeniy A. Zakharychev, Hydrogel scaffolds based on blood plasma cryoprecipitate and collagen derived from various sources: Structural, mechanical and biological characteristics, Bioactive Materials, Volume 4, 2019, Pages 334-345, ISSN 2452-199X, https://doi.org/10.1016/j.bioactmat.2019.10.003.
-
Yudin, V.V.; Kulikova, T.I.; Morozov, A.G.; Egorikhina, M.N.; Rubtsova, Y.P.; Charykova, I.N.; Linkova, D.D.; Zaslavskaya, M.I.; Farafontova, E.A.; Kovylin, R.S.; et al. Features of Changes in the Structure and Properties of a Porous Polymer Material with Antibacterial Activity during Biodegradation in an In Vitro Model. Polymers 2024, 16, 379. https://doi.org/10.3390/polym16030379
-
Aleynik, D.Y.; Bokov, A.E.; Charykova, I.N.; Rubtsova, Y.P.; Linkova, D.D.; Farafontova, E.A.; Egorikhina, M.N. Functionalization of Osteoplastic Material with Human Placental Growth Factor and Assessment of Biocompatibility of the Resulting Material In Vitro. Pharmaceutics 2024, 16, 85. https://doi.org/10.3390/pharmaceutics16010085
В лаборатории накоплен многолетний опыт проведения доклинических исследований in vitro медицинских изделий, материалов биомедицинского назначения, лекарственных препаратов и ВТЛП на основе соматических клеток и их продуктов.
Мы предлагаем широкий спектр исследований с использованием в качестве тест-систем первичных культур поверхностно-зависимых клеток человека и животных:
- Оценка цитотоксичности
- МТТ-тест
- Метод прямого контакта
- Оценка адгезивных свойств поверхности с качественной оценкой жизнеспособности
- Оценка пролиферативной активности при культивировании клеток на / в материале
- Оценка жизнеспособности при культивировании клеток на / в материале
- Оценка секреторной активности при культивировании клеток на / в материале
- Для материалов с пористой структурой:
- Оценка распределения клеток относительно внутренней структуры материала
- Оценка миграционной активности
- Возможна организация исследований in vivo на мелких и крупных лабораторных животных
Контакты:

Сотрудники
Подписывайтесь на наши социальные сети
- :
ПИМУ
только что
Свежие новости университета
Будьте в курсе всех новостей.








